地熱発電における水の状態量
水に熱を加えると温度が高くなることは誰でも経験的に知っています。コンロなどで熱を加え続ければ水の温度は次第に高くなり、やがて沸騰します。沸騰するとヤカンの口からは勢いよく湯気が噴き出すが、温度は100℃より高くなりません。沸騰している状態では外部から与えられるエネルギーは水の温度を上げることには使われず、液相から気相への状態変化に使われます。この状態を「飽和」と呼びます。
水は100℃で沸騰することが知られていますが、それは平地の大気圧でのことであり、気圧の低い高山などでは沸騰する温度は低くなります。1 気圧(1,013.25 hPa=1.01325 bar)での飽和温度は99.97℃で、ほぼ100℃です。標高2,000m 程度の高地では大気圧は0.8 bar 程度になり飽和温度は93℃、標高4,000m 程度で0.6 bar で86℃程度となります。この性質はセパレータの圧力と発生蒸気量の関係を理解するのに役立ち、ダブルフラッシュにおいて熱水の圧力を下げることにより、圧力の低い蒸気が得られることが理解できます。表1に飽和状態での圧力と温度の関係を示します。
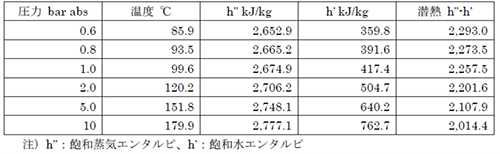
飽和状態での液相と気相のエンタルピの差を潜熱と呼ぶ。お湯を沸かしているときに100℃のお湯が100℃の蒸気に変化する際に必要なエネルギーが潜熱に相当します。1 気圧での潜熱は2,256.5kJ/kg(水のエンタルピは419.0kJ/kg、蒸気は2,675.5 kJ/kg)であり、この値は539 kcal/kg に相当します。1kg の水の温度を1℃上昇させるのに必要なエネルギーが1 kcal と定義されるので、蒸気1kg の潜熱で539kg の水の温度を1℃上げることができます。潜熱が非常に大きなエネルギーであることが想像いただけると思います。表1に潜熱を示します。この性質は冷却塔で水が冷却される原理の理解に役立ちます。
表1 を眺めると、圧力・温度が高くなるにつれて潜熱が小さくなっていることがわかります。さらに圧力・温度を高めていくと、やがて潜熱がゼロとなる状態になります。潜熱がゼロという意味は液相と気相の間にエンタルピの飛躍が無いことを示し、この潜熱がゼロとなる点を臨界点と呼び、その圧力を臨界圧力、温度を臨界温度と呼びます。臨界点以上になると気体とも液体とも異なる状態になります。水の臨界圧力は約220bar、臨界温度は374℃です。このような高温高圧の状態は地熱資源とは無縁のように思われますが、最近の深部地熱では400℃以上を目指す試みもあると伝えられており、将来は超臨界の地熱資源を扱う時代が来るかもしれません。
【参考文献】
- ・新エネルギー財団(2021):「令和2年度 地熱開発技術者研修会テキスト」



